试题详情
- 简答题试述酶促反应的动力学。
- 影响酶促反应速度的因素包括下列6种。
(1)底物浓度:在其他因素不变的情况下,底物浓度对酶反应的影响呈矩形双曲线关系。反应速度v与底物浓度[s]的关系,可用米-曼方程式表示:v=v
 [s]/k
[s]/k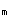 +[s]。k
+[s]。k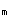 为米氏常数,它等于酶促反应最大速度(v
为米氏常数,它等于酶促反应最大速度(v )一半时的底物浓度,可近似反映酶对底物的亲和力。k
)一半时的底物浓度,可近似反映酶对底物的亲和力。k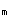 值愈小,酶与底物的亲和力愈大。同一酶对不同底物有不同的k
值愈小,酶与底物的亲和力愈大。同一酶对不同底物有不同的k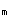 值。
(2)酶浓度:在低[s]时,酶活性中心远未被[s]饱和,v将随[s]增加而加快;当[s]>[e]时,底物占据了全部酶活性中心,即酶被底物充分饱和,其反应速度达到v
值。
(2)酶浓度:在低[s]时,酶活性中心远未被[s]饱和,v将随[s]增加而加快;当[s]>[e]时,底物占据了全部酶活性中心,即酶被底物充分饱和,其反应速度达到v ,而v将与酶浓度[e]成正比。
(3)温度:温度升高,酶促反应速度加快,由于酶的化学本质是蛋白质,当温度升达一定值时,会引起酶蛋白变性,致使其反应速度反而降低。酶促反应速度最快时的温度称为最适温度。哺乳动物体内的酶,其最适温度为35℃~40℃。
(4)ph酶分子含有许多极性基因,在不同的ph下呈不同的解离状态,所带电荷亦各异,只有当酶蛋白处于一定的解离状态,才能与底物结合,因此,ph的变化对酶的催化作用有很大影响,酶催化活性最大时的ph值称为最适ph,如胃蛋白酶的最适ph在1.5。
(5)激活剂:使酶由无活性变为有活性,或使酶活性增强的物质,称为酶的激活剂,它们大多为金属离子或有机化合物。
(6)抑制剂:酶的活性中心或必需基团的性质受到某些化学物质的影响,引起的酶活性降低或丧失,这种效应称为抑制作用(包括不可逆性抑制作用和可逆性抑制作用),而那些化学物质即为酶的抑制剂。
1)不可逆性抑制作用:抑制剂常与酶的必需基团呈共价结合,使酶丧失活性,它们不能用透析、超滤等方法去除,如对氯汞苯甲酸对含巯基酶的抑制。
2)可逆性抑制作用:抑制剂以非共价键与酶或es复合物可逆地结合,使酶的活性降低或丧失,但它们可通过透析、超滤而除去。该抑制作用又包括3个主要类型:①竞争性的抑制作用。抑制剂与底物结构相似,可竞争酶的活性中心,其抑制程度取决于抑制剂与酶的相对亲和力和底物浓度。动力学特点:v
,而v将与酶浓度[e]成正比。
(3)温度:温度升高,酶促反应速度加快,由于酶的化学本质是蛋白质,当温度升达一定值时,会引起酶蛋白变性,致使其反应速度反而降低。酶促反应速度最快时的温度称为最适温度。哺乳动物体内的酶,其最适温度为35℃~40℃。
(4)ph酶分子含有许多极性基因,在不同的ph下呈不同的解离状态,所带电荷亦各异,只有当酶蛋白处于一定的解离状态,才能与底物结合,因此,ph的变化对酶的催化作用有很大影响,酶催化活性最大时的ph值称为最适ph,如胃蛋白酶的最适ph在1.5。
(5)激活剂:使酶由无活性变为有活性,或使酶活性增强的物质,称为酶的激活剂,它们大多为金属离子或有机化合物。
(6)抑制剂:酶的活性中心或必需基团的性质受到某些化学物质的影响,引起的酶活性降低或丧失,这种效应称为抑制作用(包括不可逆性抑制作用和可逆性抑制作用),而那些化学物质即为酶的抑制剂。
1)不可逆性抑制作用:抑制剂常与酶的必需基团呈共价结合,使酶丧失活性,它们不能用透析、超滤等方法去除,如对氯汞苯甲酸对含巯基酶的抑制。
2)可逆性抑制作用:抑制剂以非共价键与酶或es复合物可逆地结合,使酶的活性降低或丧失,但它们可通过透析、超滤而除去。该抑制作用又包括3个主要类型:①竞争性的抑制作用。抑制剂与底物结构相似,可竞争酶的活性中心,其抑制程度取决于抑制剂与酶的相对亲和力和底物浓度。动力学特点:v 不变,k
不变,k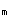 增大,斜率增大。②非竞争性抑制作用。抑制剂与酶活性中心外的必需基团结合,底物与抑制剂之间无竞争关系,其抑制程度取决于抑制剂浓度。动力学特点:v
增大,斜率增大。②非竞争性抑制作用。抑制剂与酶活性中心外的必需基团结合,底物与抑制剂之间无竞争关系,其抑制程度取决于抑制剂浓度。动力学特点:v 降低,k
降低,k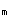 不变,斜率增大。③反竞争性抑制作用。抑制剂只与酶一底物复合物结合,其抑制程度取决于抑制剂浓度和底物浓度。动力学特点:v
不变,斜率增大。③反竞争性抑制作用。抑制剂只与酶一底物复合物结合,其抑制程度取决于抑制剂浓度和底物浓度。动力学特点:v 降低,k
降低,k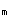 降低,斜率不变。
降低,斜率不变。 关注下方微信公众号,在线模考后查看

热门试题
- 翼点位于_____、_____、____
- 溶出度合格的制剂其崩解时限一定合格。反之
- 关于网膜孔的描述,何者错误
- 异烟肼是治疗结核病的首选药物。它有哪些优
- 药物通过生物膜转运的主要方式是主动转运。
- 肝细胞性黄疸血清中酯型胆红素_____,
- 什么是休克?引起休克的常见原因有哪些?
- 大输液中微粒来源包括________、_
- 为什么说没有游离气腹征象并不能排除胃肠道
- 医院感染主要发生在
- 肺癌早期诊断方法有哪些?
- 试述脉管系的组成。
- 何谓脑的灰质、皮质、白质、髓质、神经核?
- 用酶法检查Rh血型,与不完全抗D抗体无反
- 躯体运动神经属胆碱能神经。
- 什么是分析范围、干扰和介质效应?
- 输注血浆有些什么副作用?
- 试述医院感染的诊断原则。
- Ⅰ型呼吸衰竭与Ⅱ型呼吸衰竭各有什么血气特
- 下列药物为保钾利尿药